Thème de recherche Douleur et vieillissement
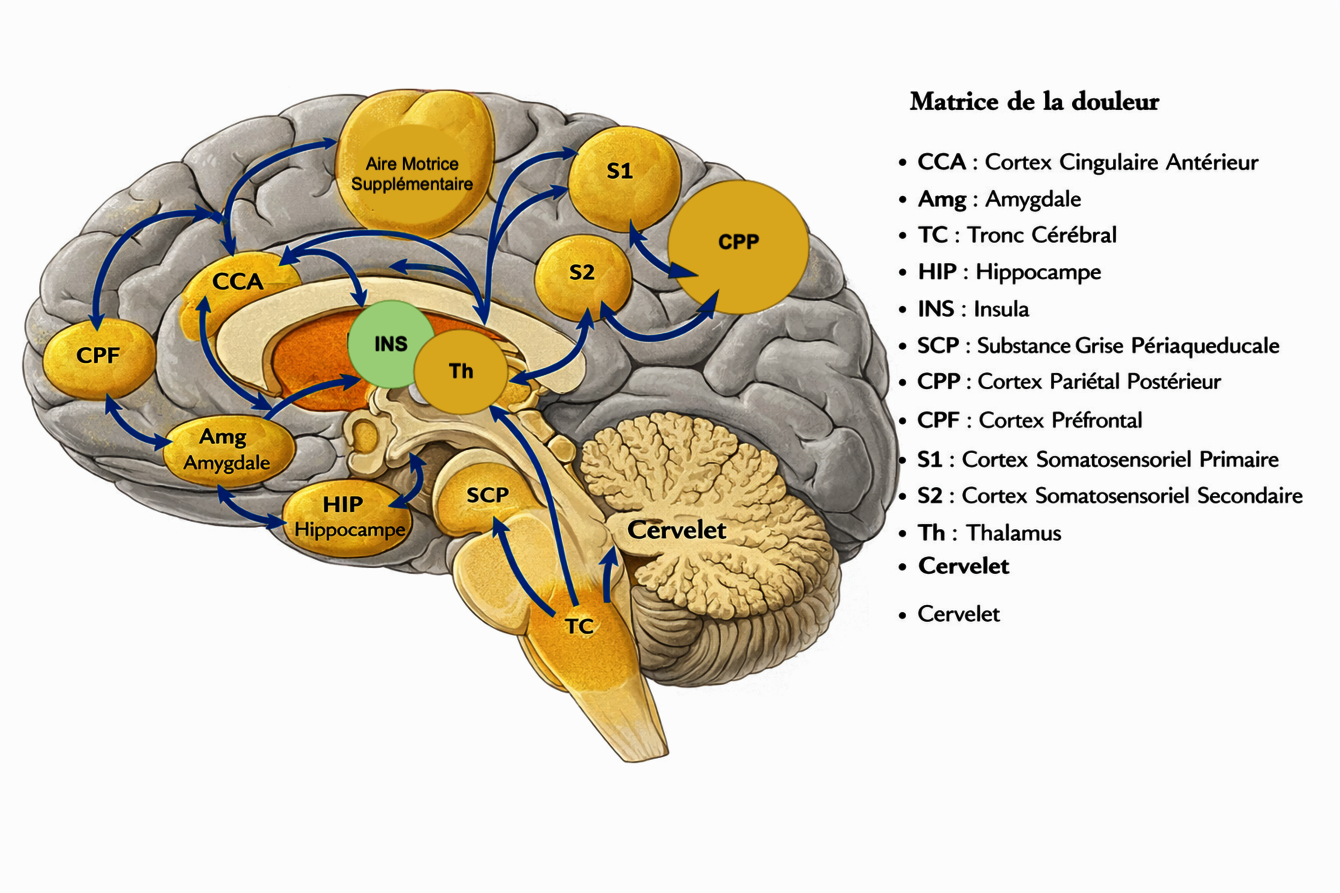
Les douleurs chroniques touchent près d’une personne âgée sur deux et constituent un enjeu majeur de santé publique. Une partie de nos travaux vise à comprendre les mécanismes cognitifs et les mécanismes cérébraux impliqués dans la modulation de la douleur au cours du vieillissement, en particulier le rôle des fonctions exécutives et des mécanismes d’inhibition endogène descendante de la douleur. L’altération des réseaux préfrontaux avec l’âge pourrait ainsi contribuer à une diminution de la capacité à moduler cognitivement la douleur. Nous étudions ces mécanismes à l’aide de modèles expérimentaux de douleur tonique, en lien avec le niveau de fonctionnement cognitif des participants.
Nos recherches portent également sur l’étude des modifications des voies nociceptives et somatosensorielles liées à l’âge. Elles s’appuient sur des approches multimodales combinant méthodes psychophysiques, stimulation sensorielle contrôlée et enregistrements neurophysiologiques. Ces travaux visent à caractériser le fonctionnement des voies thermo-nociceptives et tactiles, ainsi que les interactions entre modalités sensorielles, afin de mieux comprendre les mécanismes périphériques et centraux impliqués dans la perception douloureuse au cours du vieillissement. Enfin, nous nous intéressons aux douleurs neuropathiques, notamment dans le contexte du diabète de type II. Le diabète constitue un modèle d’atteinte progressive des voies somatosensorielles, associant des altérations des fibres nociceptives et non nociceptives. Nos études visent à mieux caractériser les mécanismes sensoriels et centraux impliqués dans ces douleurs, et à améliorer leur évaluation à l’aide d’outils psychophysiques et neurophysiologiques.
Axes de recherche
Modification de l’inhibition endogène de la douleur avec l’âge
Modification des voies nociceptives avec l’âge
Douleurs neuropathiques dans le diabète de type II